例1、(福建福州)人类生活离不开金属。
(1)铁是生活中常用的金属。下图是某“取暖片”外包装的图片。该“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热。

①发热剂需接触到空气才会发热,原因是铁要与______________、____________等物质共同作用才会生锈。
②推测发热剂成分中氯化钠的作用是_________________________。
(2)应用金属活动性顺序表能帮助我们进一步学习金属性质。
已知下列各组物质间均能发生置换反应。
A.Fe和CuSO4溶液 B.Mg和MnSO4溶液 C.Mn和FeSO4溶液
①写出Fe和CuSO4溶液反应的化学方程式___________。
②Mn、Fe、Mg、Cu四种金属的活动性由强到弱的顺序_______________。
解析:
铁生锈需要两个条件:一是与氧气接触;二是与水接触。在发热剂中加入氯化钠,实际上增强水的导电能力,加快铁粉生锈,更快的放出热量。根据金属与盐的置换反应规律,可得到金属的相对活动性顺序。
答案:
(1)①水、氧气
②加速铁粉生锈,更快的放出热量
(2)①Fe+CuSO4=FeSO4+Cu
②Mg、Mn、Fe、Cu
例2、(北京)铜和铁是生产、生活中广泛使用的金属。
(1)工业上用一氧化碳和赤铁矿(主要成分是氧化铁)冶炼铁,反应的化学方程式为_____________________。
(2)铁生锈的条件是_______________;铜表面也容易生成绿色铜锈,铜锈的主要成分是碱式碳酸铜,化学式为Cu2(OH)2CO3,其组成元素有___________种。
(3)老师用生锈的铜片、铁粉和稀硫酸进行实验,实验过程如下图所示(部分生成物已略去)。
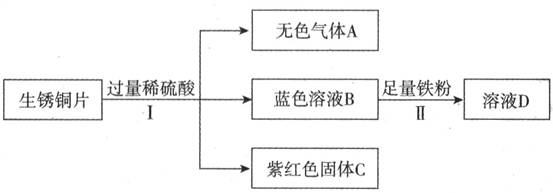
①紫红色固体C的化学式为_______________
②写出Ⅱ中反应的化学方程式________________
解析:
(3)①生锈铜片表面的物质被稀硫酸除去后,就得到紫红色固体Cu,因为Cu不活泼,不和稀硫酸反应。②蓝色溶液为CuSO4,加入铁粉后,发生了反应:Fe+CuSO4=Cu+FeSO4,又因为硫酸是过量的,所以还有反应Fe+H2SO4=FeSO4+H2↑发生。
答案:
(1)3CO+Fe2O3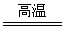 2Fe+3CO2
2Fe+3CO2
(2)与潮湿空气接触;4
(3)①Cu
②Fe+CuSO4=FeSO4+Cu;Fe+H2SO4=FeSO4+H2↑
例3、(南昌市)请你参与某学习小组的探究活动,并回答相关问题:
发现问题
小丽发现盛水的铁锅与水面接触的部分最易生锈;
小茜发现自己的铜制镜框表面出现了绿色的铜锈;
小玲发现苹果切开不久,果肉上产生一层咖啡色物质,好像生了“锈”一样。
提出问题
这三种物质“生锈”的原因是什么?
收集证据
(1)回忆已学知识,铁生锈的条件是_______________________。
(2)查阅有关资料:“铜锈”主要成分是Cu2(OH)2CO3(俗称铜绿);苹果“生锈”是果肉里的物质(酚和酶)与空气中氧气发生了一系列的反应,生成咖啡色物质。
(3)实验探究:将四小块铜片分别按下图的示放置一个月,观察现象如下表所示。
由实验可知:铜生锈是铜与水______、_______等物质共同作用的结果。
得出结论
经过交流讨论,三位同学认为这些物质“生锈”除了可能与水有关外,还可能都与_______(填物质名称)有关。
反思与应用
(1)写出一种防止铁或铜等金属制品生锈的具体方法____________;
(2)请你提出一条延长食品保质期的建议________________________。
解析:
铁生锈的条件是与水和氧气同时接触;铜在缺少水或CO2或O2时,不生锈,所以铜生锈的条件是铜与水、CO2、O2同时接触;保护金属制品不被锈蚀的方法是保持其表面干燥、洁净或在其表面形成保护膜,而食品保质需要隔绝空气。
答案:
收集证据:(1)铁与氧气和水同时接触(2)氧气 、 二氧化碳
得出结论:氧气
反思与应用:
(1)保持金属制品表面的洁净和干燥(或表面形成保护膜)
(2)将食品进行真空包装(或充入氮气等)。
例4、(佛山市)有X、Y、Z三种金属,只有Z能与稀H2SO4反应,当把Y放入X的盐溶液,Y表面有X析出,则这三种金属的活动性顺序是( )
A.Z>Y>X B.X>Z>Y C.Y>X>Z D.Y>Z>X
解析:
在金属活动性顺序里,排在前面的金属能将排在它后面的金属从它们的盐溶液中置换出来。只有Z能与稀H2SO4反应,说明Z>H,而Y能与X的盐溶液反应,说明Y>X,故Z>Y>X.
答案:A
例5、(河北省)某化学兴趣小组,为验证Fe、Cu、Ag三种金属活动性顺序,设计了如图所示的4种实验方案。其中不能达到目的的是( )