| 离子(2) |
主讲: 化学高级教师 舒宝生
一、离子
带电荷的原子(或原子团)叫做离子,如Na+、Cl-、SO42-等。
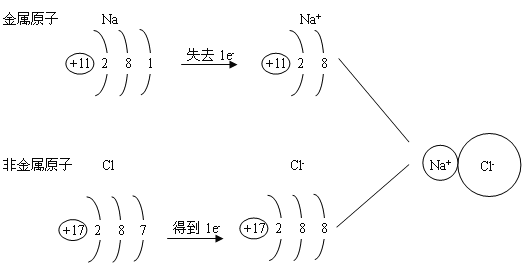
1、离子的形成
2、离子的分类
阳离子:带正电荷的原子(或原子团),核电荷数>核外电子数
如Na+、Mg2+、NH4+
阴离子:带负电荷的原子(或原子团),核电荷数<核外电子数
如Cl-、S2-、SO42-
3、离子符号的书写
(1)先写出元素符号,然后在右上角标上离子所带电荷数,数目在前,正负号在后。离子带1个单位正电荷或1个单位负电荷时,“1”省略不写。如Na+、Cl-、Mg2+、S2-、SO42-等。
(2)离子所带的电荷数等于原子得到或失去电子的数目。
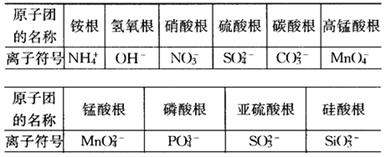
(3)常见原子团形成的离子
4、离子符号的意义
表示某种离子;表示某元素的一个离子。
如:“Mg2+”的含义为:①1个镁离子;②1个镁离子带2个单位的正电荷。
注意:
①离子符号中数字的意义:表示某种离子所带的电荷数,如“Mg2+”中“2”的含义表示一个镁离子带2个单位的正电荷。
②在离子符号前加上系数后,就只能表示离子的个数,如“3Mg2+”只能表示3个镁离子。
二、构成物质的粒子
1、分子:一部分单质和化合物是由分子构成的,如氢气(H2)、氧气(O2)、水(H2O)等。
2、原子:金属、固态非金属(有例外,如碘)、稀有气体是由原子直接构成的。
3、离子:离子化合物均由离子构成,如氯化钠,典型的金属元素(如Na、Mg等)与典型的非金属元素(如F、O、Cl、S等)形成的化合物均是离子化合物。
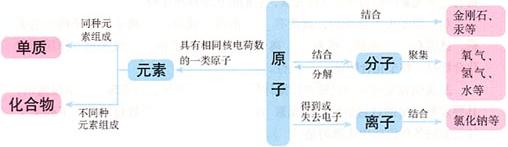
【讲解】物质与其构成粒子之间的关系
- 返回 -